Nozokomiálna pneumónia je najčastejšou a najzávažnejšou nozokomiálnou infekciou, z ktorej pneumónia spojená s umelou pľúcnou ventiláciou (VAP) predstavuje 40 %. VAP spôsobená refraktérnymi patogénmi je stále zložitým klinickým problémom. Už roky odporúčajú smernice celý rad intervencií (ako je cielená sedácia, elevácia hlavy) na prevenciu VAP, ale VAP sa vyskytuje až u 40 % pacientov s tracheálnou intubáciou, čo vedie k dlhším hospitalizáciám, zvýšenému užívaniu antibiotík a úmrtiu. Ľudia neustále hľadajú účinnejšie preventívne opatrenia.
Pneumónia spojená s umelou pľúcnou ventiláciou (VAP) je nový vznik pneumónie, ktorá sa vyvíja 48 hodín po tracheálnej intubácii a je najčastejšou a smrteľnou nozokomiálnou infekciou na jednotke intenzívnej starostlivosti (JIS). Usmernenia Americkej spoločnosti pre infekčné choroby z roku 2016 rozlišujú VAP od definície nozokomiálnej pneumónie (HAP) (HAP sa vzťahuje iba na pneumóniu, ktorá sa vyskytuje po hospitalizácii bez tracheálnej kanyly a nesúvisí s mechanickou ventiláciou; VAP je pneumónia po tracheálnej intubácii a mechanickej ventilácii) a Európska spoločnosť a Čína sa domnievajú, že VAP je stále špeciálnym typom HAP [1-3].
U pacientov na mechanickej ventilácii sa výskyt VAP pohybuje od 9 % do 27 %, úmrtnosť sa odhaduje na 13 % a môže viesť k zvýšenému systémovému užívaniu antibiotík, predĺženej mechanickej ventilácii, predĺženému pobytu na JIS a zvýšeným nákladom [4-6]. HAP/VAP u pacientov bez imunodeficiencie je zvyčajne spôsobená bakteriálnou infekciou a distribúcia bežných patogénov a ich charakteristiky rezistencie sa líšia v závislosti od regiónu, triedy nemocnice, populácie pacientov a expozície antibiotikám a menia sa v priebehu času. Pseudomonas aeruginosa dominovala patogénom súvisiacim s VAP v Európe a Amerike, zatiaľ čo v terciárnych nemocniciach v Číne bolo izolovaných viac Acinetobacter baumannii. Tretina až polovica všetkých úmrtí súvisiacich s VAP je priamo spôsobená infekciou, pričom úmrtnosť prípadov spôsobených Pseudomonas aeruginosa a acinetobacterom je vyššia [7,8].
Vzhľadom na silnú heterogenitu VAP je diagnostická špecifickosť jej klinických prejavov, zobrazovacích a laboratórnych testov nízka a rozsah diferenciálnej diagnostiky je široký, čo sťažuje včasnú diagnostiku VAP. Zároveň bakteriálna rezistencia predstavuje vážnu výzvu pre liečbu VAP. Odhaduje sa, že riziko vzniku VAP je 3 %/deň počas prvých 5 dní používania mechanickej ventilácie, 2 %/deň medzi 5. a 10. dňom a 1 %/deň počas zvyšku času. Vrchol incidencie sa zvyčajne vyskytuje po 7 dňoch ventilácie, takže existuje okno, v ktorom je možné infekcii včas predísť [9,10]. Mnohé štúdie sa zamerali na prevenciu VAP, ale napriek desaťročiam výskumu a pokusom o prevenciu VAP (ako je vyhýbanie sa intubácii, predchádzanie reintubácii, zníženie sedácie, zdvihnutie hlavy postele o 30° až 45° a starostlivosť o ústnu dutinu) sa zdá, že incidencia sa neznížila a súvisiaca lekárska záťaž zostáva veľmi vysoká.
Inhalačné antibiotiká sa používajú na liečbu chronických infekcií dýchacích ciest od 40. rokov 20. storočia. Keďže dokážu maximalizovať dodávanie liekov do cieľového miesta infekcie (t. j. dýchacích ciest) a znížiť systémové vedľajšie účinky, preukázali dobrú aplikačnú hodnotu pri rôznych ochoreniach. Inhalačné antibiotiká sú teraz schválené americkým Úradom pre kontrolu potravín a liečiv (FDA) a Európskou agentúrou pre lieky (EMA) na použitie pri cystickej fibróze. Inhalačné antibiotiká môžu významne znížiť bakteriálnu záťaž a frekvenciu exacerbácií pri bronchiektázii bez zvýšenia celkových nežiaducich udalostí a súčasné usmernenia ich uznávajú ako liečbu prvej voľby u pacientov s infekciou Pseudomonas aeruginosa a častými exacerbáciami. Inhalačné antibiotiká počas perioperačného obdobia transplantácie pľúc sa môžu použiť aj ako adjuvantné alebo profylaktické lieky [11,12]. V usmerneniach pre VAP v USA z roku 2016 však odborníci nemali dôveru v účinnosť adjuvantných inhalačných antibiotík kvôli nedostatku rozsiahlych randomizovaných kontrolovaných štúdií. Štúdia fázy 3 (INHALE) publikovaná v roku 2020 tiež nepriniesla pozitívne výsledky (inhalácia amikacínu s asistenciou intravenóznych antibiotík pri gramnegatívnej bakteriálnej infekcii spôsobenej pacientmi s VAP, dvojito zaslepená, randomizovaná, placebom kontrolovaná štúdia účinnosti fázy 3, celkovo 807 pacientov, systémová liečba + asistovaná inhalácia amikacínu počas 10 dní).
V tejto súvislosti tím vedený výskumníkmi z Regionálnej univerzitnej nemocnice v Tours (CHRU) vo Francúzsku prijal odlišnú výskumnú stratégiu a vykonal multicentrickú, dvojito zaslepenú, randomizovanú kontrolovanú štúdiu účinnosti (AMIKINHAL) iniciovanú skúšajúcim. Inhalačný amikacín alebo placebo na prevenciu VAP boli porovnávané na 19 jednotkách intenzívnej starostlivosti vo Francúzsku [13].
Celkovo 847 dospelých pacientov s invazívnou mechanickou ventiláciou medzi 72 a 96 hodinami bolo náhodne rozdelených v pomere 1:1 do skupín s inhaláciou amikacínu (N = 417, 20 mg/kg ideálnej telesnej hmotnosti, QD) alebo inhaláciou placeba (N = 430, ekvivalent 0,9 % chloridu sodného) počas 3 dní. Primárnym koncovým ukazovateľom bola prvá epizóda VAP od začiatku randomizovaného zaradenia do 28. dňa.
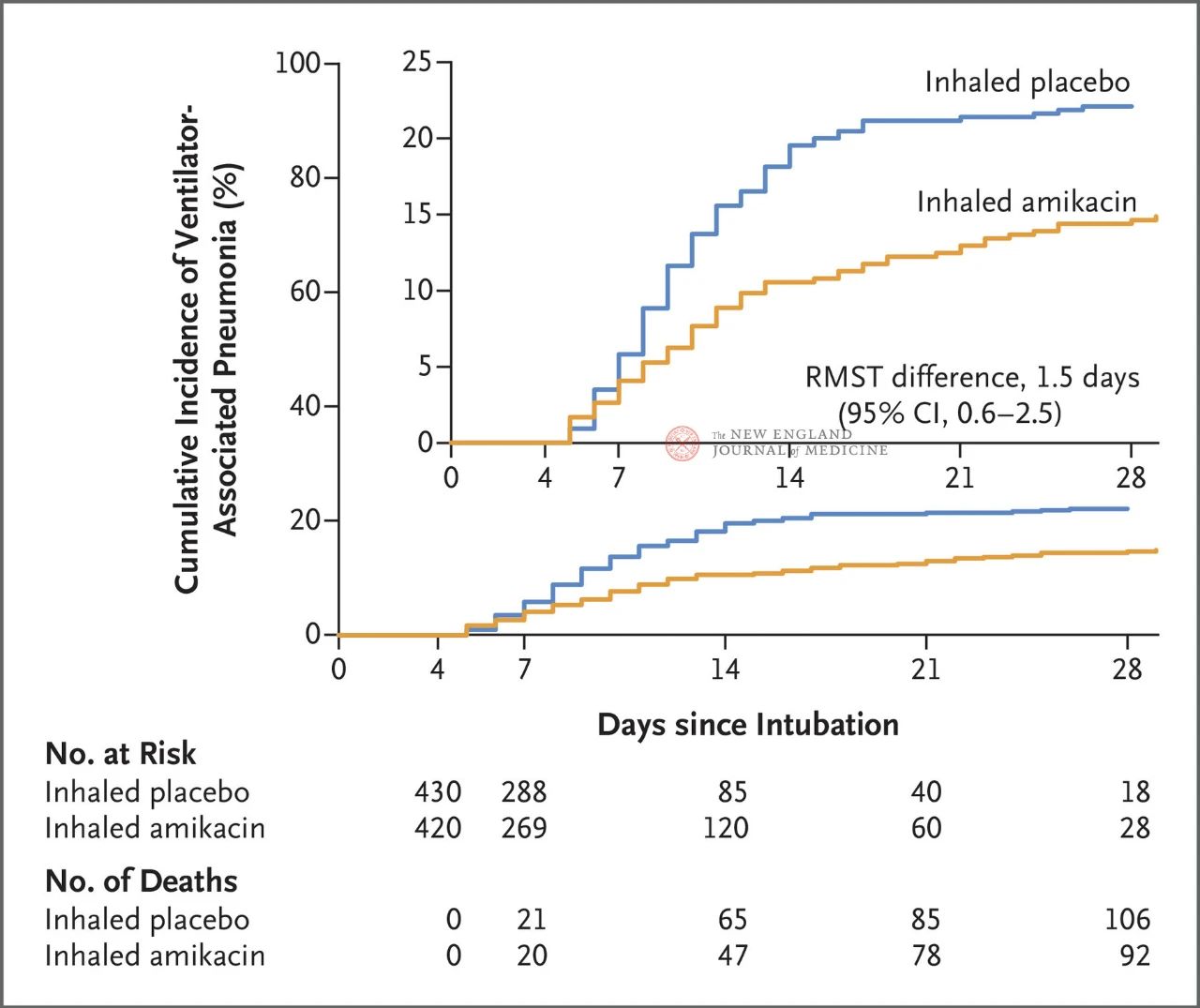
Výsledky štúdie ukázali, že po 28 dňoch sa u 62 pacientov (15 %) v skupine s amikacínom vyvinula VAP a u 95 pacientov (22 %) v skupine s placebom sa vyvinula VAP (obmedzený priemerný rozdiel v prežívaní pre VAP bol 1,5 dňa; 95 % CI, 0,6 – 2,5; P = 0,004).
Z hľadiska bezpečnosti sa u siedmich pacientov (1,7 %) v skupine s amikacínom a u štyroch pacientov (0,9 %) v skupine s placebom vyskytli závažné nežiaduce udalosti súvisiace so štúdiou. Spomedzi tých, ktorí nemali akútne poškodenie obličiek pri randomizácii, malo 11 pacientov (4 %) v skupine s amikacínom a 24 pacientov (8 %) v skupine s placebom akútne poškodenie obličiek na 28. deň (HR 0,47; 95 % CI 0,23 – 0,96).
Klinická štúdia mala tri hlavné body. Po prvé, z hľadiska dizajnu štúdie, štúdia AMIKINHAL vychádza zo štúdie IASIS (randomizovaná, dvojito zaslepená, placebom kontrolovaná, paralelná štúdia fázy 2 zahŕňajúca 143 pacientov). Na vyhodnotenie bezpečnosti a účinnosti inhalačnej systémovej liečby infekcie gramnegatívnymi baktériami spôsobenej VAP sa použili amikacín-fosfomycín na systémovú liečbu infekcie spôsobenej VAP a štúdie INHALE, ktorá sa skončila s negatívnymi výsledkami a zameriava sa na prevenciu VAP, pričom sa dosiahli relatívne dobré výsledky. Vzhľadom na charakteristiky vysokej úmrtnosti a dlhej hospitalizácie u pacientov s mechanickou ventiláciou a VAP, ak inhalácia amikacínu dokáže dosiahnuť výrazne odlišné výsledky v znižovaní úmrtnosti a hospitalizácie u týchto pacientov, bude cennejšia pre klinickú prax. Vzhľadom na heterogenitu neskorej liečby a starostlivosti u každého pacienta a každého centra však existuje množstvo mätúcich faktorov, ktoré môžu štúdiu ovplyvňovať, takže môže byť ťažké dosiahnuť pozitívny výsledok, ktorý sa pripisuje inhalačným antibiotikám. Úspešná klinická štúdia si preto vyžaduje nielen vynikajúci dizajn štúdie, ale aj výber vhodných primárnych koncových bodov.
Po druhé, hoci sa aminoglykozidové antibiotiká v rôznych smerniciach pre VAP neodporúčajú ako samostatné liečivo, aminoglykozidové antibiotiká môžu pokrývať bežné patogény u pacientov s VAP (vrátane Pseudomonas aeruginosa, acinetobacter atď.) a to kvôli ich obmedzenej absorpcii v pľúcnych epitelových bunkách, vysokej koncentrácii v mieste infekcie a nízkej systémovej toxicite. Aminoglykozidové antibiotiká sú medzi inhalačnými antibiotikami široko uprednostňované. Táto práca je v súlade s komplexným odhadom veľkosti účinku intratracheálneho podania gentamicínu v malých vzorkách publikovaným skôr, čo spoločne demonštruje účinok inhalačných aminoglykozidových antibiotík na prevenciu VAP. Treba tiež poznamenať, že väčšina placebových kontrol vybraných v štúdiách súvisiacich s inhalačnými antibiotikami je fyziologický roztok. Vzhľadom na to, že atomizovaná inhalácia samotného fyziologického roztoku môže zohrávať určitú úlohu pri riedení spúta a pomáhať pri expektorancii, fyziologický roztok môže spôsobiť určité rušenie v analýze výsledkov štúdie, čo by sa malo v štúdii komplexne zohľadniť.
Okrem toho je dôležitá lokálna adaptácia liekov HAP/VAP, rovnako ako antibiotická profylaxia. Zároveň, bez ohľadu na dĺžku intubácie, je ekológia miestnej JIS najdôležitejším rizikovým faktorom infekcie baktériami rezistentnými voči viacerým liekom. Preto by sa empirická liečba mala čo najviac odvolávať na mikrobiologické údaje miestnych nemocníc a nemala by sa slepo odvolávať na smernice alebo skúsenosti terciárnych nemocníc. Zároveň kriticky chorí pacienti vyžadujúci mechanickú ventiláciu majú často kombinované multisystémové ochorenia a pri kombinovanom pôsobení viacerých faktorov, ako je stresový stav, môže dôjsť aj k fenoménu presluchu črevných mikróbov do pľúc. Vysoká heterogenita ochorení spôsobená vnútornou a vonkajšou superpozíciou tiež určuje, že rozsiahla klinická propagácia každého nového zásahu je ešte dlhá cesta.
Čas uverejnenia: 2. decembra 2023